
Axit nitric HNO3 là gì? Tìm hiểu tính chất và ứng dụng
16 Tháng 12, 2024
- 1. Axit nitric HNO3 là gì?
- 2. Công thức cấu tạo của HNO3
- 3. Tính chất của axit nitric
- 3.1. Tính chất vật lý
- 3.2. Tính chất hóa học
- 4. Ứng dụng của axit nitric
- 5. Điều chế axit nitric
- 5.1. Phương pháp Ostwald
- 5.2. Phương pháp phản ứng nitrat kim loại với axit sunfuric
- 6. Thắc mắc thường gặp về axit nitric
- 6.1. HNO3 là axit mạnh hay yếu?
- 6.2. HNO3 làm quỳ tím chuyển màu gì?
- 6.3. Axit nitric có độc không?
Axit nitric (HNO3) là một trong những hợp chất hóa học quan trọng và phổ biến trong ngành công nghiệp. Với đặc tính mạnh mẽ và tính ăn mòn cao, axit nitric không chỉ được sử dụng trong sản xuất phân bón mà còn đóng vai trò quan trọng trong nhiều lĩnh vực khác như chế tạo thuốc nổ, xử lý kim loại, và sản xuất các hợp chất hóa học. Vậy axit nitric là gì? Tính chất và ứng dụng của nó như thế nào? Cùng GH group tìm hiểu chi tiết về loại axit này qua bài viết dưới đây.
1. Axit nitric HNO3 là gì?

Axit Nitric
Axit nitric (HNO3) là một hợp chất hóa học vô cơ, có công thức hóa học là HNO3. Đây là một axit mạnh, được biết đến với tên gọi khác như dung dịch nitrat hidro hay axit nitric khan. Axit này tồn tại dưới dạng chất lỏng không màu, dễ bay hơi và có tính ăn mòn cao.
Trong tự nhiên, HNO3 được hình thành thông qua các phản ứng hóa học xảy ra trong khí quyển. Khi sấm sét hoặc tia chớp xuất hiện, chúng tạo ra năng lượng kích thích các phân tử nitơ và oxy trong không khí phản ứng với nhau, sau đó hòa tan vào nước mưa, tạo thành axit nitric. Đây chính là lý do vì sao người ta thường nói rằng axit nitric có thể xuất hiện từ những cơn mưa do sấm và sét.
Với đặc tính hóa học và vai trò quan trọng trong nhiều lĩnh vực, HNO3 đã trở thành một trong những hóa chất không thể thiếu trong công nghiệp, nông nghiệp và nghiên cứu khoa học.
2. Công thức cấu tạo của HNO3
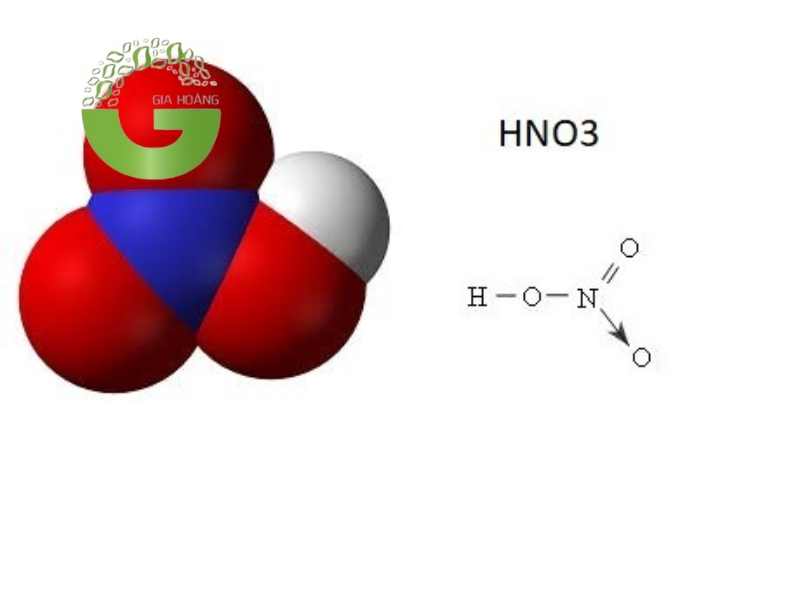
Công thức cấu tạo HNO3
Trong phân tử HNO3, nguyên tử nitơ (N) nằm ở trung tâm, liên kết với ba nguyên tử oxy (O) và một nguyên tử hydro (H). Cụ thể:
- Nguyên tử nitơ (N) liên kết đôi với một nguyên tử oxy (O), tạo thành liên kết đôi N=O.
- Một nguyên tử oxy khác liên kết đơn với nitơ và mang một điện tích âm, tạo thành nhóm ion nitrat (-NO3).
- Nguyên tử hydro (H) liên kết với một nguyên tử oxy thông qua liên kết hydro, tạo thành nhóm -OH.
Cấu trúc này giúp HNO3 có tính chất hóa học đặc trưng của một axit mạnh, dễ phân ly trong nước để giải phóng ion H+ (proton) và ion NO3- (nitrat).
3. Tính chất của axit nitric
3.1. Tính chất vật lý

Tính chất vật lý của Axit Nitric HNO3
Axit nitric (HNO3) là một chất lỏng hoặc khí không màu, dễ bay hơi và tan nhanh trong nước với nồng độ tối đa khoảng 65%. Tuy nhiên, trong tự nhiên, HNO3 thường có màu vàng nhạt do sự tích tụ của các oxit nitơ (NOx). Đây là một axit mạnh, có tính ăn mòn cao, dễ bắt lửa và cực kỳ độc hại.
Một số đặc điểm vật lý nổi bật của HNO3 bao gồm:
- Tỷ trọng: Axit nitric tinh khiết có tỷ trọng là 1511 kg/m³.
- Nhiệt độ đông đặc: -41°C.
- Nhiệt độ sôi: 83°C.
- Tính dễ bay hơi: Ở nồng độ 86%, HNO3 khi để ngoài không khí sẽ xuất hiện hiện tượng khói trắng bốc lên.
Dưới tác dụng của ánh sáng, Axit nitric dễ bị phân hủy, tạo ra khí nitơ dioxit (NO2), nước và oxy. Phản ứng phân hủy này diễn ra ngay cả ở nhiệt độ thường:
4HNO3→4NO2+2H2O+O2
Vì lý do này, HNO3 cần được bảo quản trong các chai lọ tối màu, tránh ánh sáng trực tiếp và lưu trữ ở nhiệt độ dưới 0°C để hạn chế sự phân hủy.
Ngoài ra, Axit Nitric có khả năng hòa tan khí NO2, tạo thành dung dịch có màu vàng hoặc đỏ ở nhiệt độ cao. Điều này ảnh hưởng đến các đặc tính vật lý như màu sắc, áp suất hơi, và nhiệt độ sôi của dung dịch. Khi chưng cất hỗn hợp HNO3 và H2O, ta thu được hỗn hợp azeotrope với nồng độ 68% HNO3 và nhiệt độ sôi là 120,5°C ở áp suất 1 atm.
3.2. Tính chất hóa học

Tính chất hóa học của Axit Nitric
Axit nitric (HNO3) là một monoaxit mạnh và có tính oxy hóa mạnh, với hằng số cân bằng axit (pKa) = -2. Trong dung dịch, HNO3 phân ly hoàn toàn thành ion nitrat (NO3⁻) và ion hiđroni (H3O⁺):
HNO3+H2O→H3O + +NO3 -
Một số tính chất hóa học của Axit Nitric :
- Tác dụng với chất chỉ thị: Axit nitric làm quỳ tím chuyển sang màu đỏ, thể hiện tính axit mạnh.
- Tác dụng với bazơ, oxit bazơ và muối cacbonat: HNO3 phản ứng với các chất này để tạo thành muối nitrat và các sản phẩm phụ như nước hoặc khí CO2:
2HNO3+CuO→Cu(NO3)2+H2O
2HNO3+Mg(OH)2→Mg(NO3)2+2H2O
2HNO3+CaCO3→Ca(NO3)2+H2O+CO2
-
Tác dụng với kim loại: HNO3 phản ứng với hầu hết các kim loại (trừ vàng và bạch kim) để tạo thành muối nitrat và các sản phẩm phụ khác như NO, NO2, hoặc H2:
- Với HNO3 đặc: Kimloại+HNO3đặc→Muối initrat+NO2+H2O
- Với HNO3 loãng: Kimloại+HNO3 loãng→Muối initrat+NO+H2O
- Ví dụ: Mg+2HNO3 loãng lạnh→Mg(NO3)2+H2
- Tác dụng với phi kim: HNO3 phản ứng với các phi kim (trừ silic và halogen) để tạo thành oxit nitơ và các sản phẩm khác:
C+4HNO3đặc→4NO2+2H2O+CO2
P+5HNO3đặc→5NO2+H2O+H3PO4
- Tác dụng với hợp chất hữu cơ: HNO3 có khả năng phá hủy nhiều hợp chất hữu cơ, do đó rất nguy hiểm khi tiếp xúc với cơ thể người.
- Tác dụng với hợp chất vô cơ: HNO3 phản ứng với oxit bazơ, muối hoặc các hợp chất chưa đạt hóa trị cao nhất:
FeO+4HNO3→Fe(NO3)3+NO2+2H2O
PbS+8HNO3đặc→PbSO4(kết tủa)+8NO2+4H2O
Những tính chất hóa học này giải thích tại sao HNO3 được sử dụng rộng rãi trong công nghiệp và nghiên cứu, đặc biệt trong các phản ứng nitrat hóa và sản xuất muối nitrat.
Xem thêm: Kali hidroxit KOH là gì? Tìm hiểu tính chất và ứng dụng
4. Ứng dụng của axit nitric
Sản xuất phân bón
Một trong những ứng dụng lớn nhất của HNO3 là trong sản xuất phân bón, đặc biệt là phân đạm như amoni nitrat (NH4NO3). Phân đạm này cung cấp nguồn nitơ cần thiết cho cây trồng, giúp tăng năng suất nông nghiệp. Quá trình sản xuất amoni nitrat sử dụng Axit Nitric để phản ứng với amoniac (NH3), tạo ra sản phẩm cuối cùng:
NH3+HNO3→NH4NO3
Phân bón chứa amoni nitrat không chỉ được sử dụng rộng rãi trong nông nghiệp mà còn có vai trò quan trọng trong việc cải thiện chất lượng đất và thúc đẩy sự phát triển của cây trồng.
Sản xuất thuốc nổ
Axit nitric là nguyên liệu chính trong sản xuất thuốc nổ, bao gồm các hợp chất như nitroglycerin, TNT (trinitrotoluene) và axit picric. Trong quá trình này, HNO3 được sử dụng để thực hiện phản ứng nitrat hóa, thêm nhóm nitro (-NO2) vào các hợp chất hữu cơ. Ví dụ, trong sản xuất TNT:
C6H5CH3+3HNO3→C6H2(NO2)3CH3+3H2O
Các sản phẩm này được ứng dụng trong ngành công nghiệp khai thác, xây dựng và quân sự. Tuy nhiên, do tính chất nguy hiểm của thuốc nổ, việc sử dụng HNO3 trong lĩnh vực này đòi hỏi các biện pháp an toàn nghiêm ngặt.
Công nghiệp hóa chất
Trong công nghiệp hóa chất, HNO3 đóng vai trò quan trọng trong sản xuất nhiều hợp chất hữu cơ và vô cơ. Một số ứng dụng tiêu biểu bao gồm:
- Sản xuất dược phẩm: HNO3 được sử dụng để tổng hợp các hợp chất trung gian trong sản xuất thuốc.
- Sản xuất thuốc nhuộm: Axit nitric tham gia vào các phản ứng nitrat hóa để tạo ra các hợp chất hữu cơ có màu sắc đặc trưng.
- Sản xuất nhựa và polymer: Một số loại polymer đặc biệt được sản xuất thông qua các phản ứng hóa học có sự tham gia của HNO3.
Xử lý bề mặt kim loại
HNO3 được sử dụng rộng rãi trong việc tẩy rửa và làm sạch bề mặt kim loại. Axit này giúp loại bỏ các lớp oxit, gỉ sét và tạp chất trên bề mặt kim loại, làm cho chúng sáng bóng và sạch sẽ. Quá trình này thường được áp dụng trong:
- Xử lý thép không gỉ: Làm sạch bề mặt thép trước khi gia công hoặc mạ.
- Sản xuất đồ trang sức và đồ dùng kim loại: Giúp tăng tính thẩm mỹ và độ bền của sản phẩm.
Ngoài ra, HNO3 còn được sử dụng trong các quy trình khắc axit (etching) để tạo ra các hoa văn hoặc chi tiết trên bề mặt kim loại.
5. Điều chế axit nitric
5.1. Phương pháp Ostwald

Phương pháp Ostwald điều chế HNO3
Phương pháp Ostwald là phương pháp sản xuất công nghiệp chính để điều chế HNO3 hiện nay. Quá trình này bao gồm ba giai đoạn chính, sử dụng amoniac (NH3) làm nguyên liệu đầu vào và oxy (O2) làm chất oxy hóa, với sự có mặt của xúc tác platin (Pt) hoặc rhodium (Rh). Các bước cụ thể như sau:
- Oxy hóa amoniac (NH3): Amoniac được oxy hóa trong điều kiện nhiệt độ cao (800-900°C) và áp suất, với xúc tác Pt hoặc Rh, tạo ra khí nitơ monoxide (NO): 4NH3+5O2→4NO+6H2O
- Oxy hóa nitơ monoxide (NO): Khí NO tiếp tục được oxy hóa với oxy trong không khí để tạo ra nitơ dioxit (NO2): 2NO+O2→2NO2
- Hòa tan nitơ dioxit (NO2) trong nước: NO2 được hấp thụ vào nước, tạo thành axit nitric và giải phóng khí NO (khí NO sau đó được tái sử dụng trong chu trình): 3NO2+H2O→2HNO3+NO
Phương pháp Ostwald là một quy trình hiệu quả, được sử dụng rộng rãi trong công nghiệp để sản xuất HNO3 với quy mô lớn, đáp ứng nhu cầu của nhiều ngành công nghiệp như sản xuất phân bón, thuốc nổ và hóa chất.
5.2. Phương pháp phản ứng nitrat kim loại với axit sunfuric

Phương pháp phản ứng nitrat kim loại với axit sunfuric
Phương pháp này thường được sử dụng trong phòng thí nghiệm để điều chế HNO3 với lượng nhỏ. Quá trình này dựa trên phản ứng giữa muối nitrat kim loại (ví dụ: NaNO3) và axit sunfuric (H2SO4) đậm đặc. Phản ứng tạo ra HNO3 và một muối axit sunfat: NaNO3+H2SO4→HNO3+NaHSO4
Trong phản ứng này:
- NaNO3 (natri nitrat) đóng vai trò là nguồn cung cấp ion nitrat (NO3⁻).
- H2SO4 đậm đặc đóng vai trò là chất xúc tác và chất phản ứng.
HNO3 thu được thường ở dạng hơi, sau đó được làm lạnh để ngưng tụ thành chất lỏng. Phương pháp này phù hợp cho các thí nghiệm nhỏ trong phòng thí nghiệm, nhưng không hiệu quả để sản xuất công nghiệp do chi phí cao và sản lượng thấp.
6. Thắc mắc thường gặp về axit nitric
6.1. HNO3 là axit mạnh hay yếu?

HNO3 là axit mạnh
HNO3 là một axit mạnh. Điều này có nghĩa là nó phân ly hoàn toàn trong nước, tạo ra ion H+ (hay H3O⁺) và ion NO3⁻. Với hằng số cân bằng axit (pKa) = -2, HNO3 thể hiện tính axit rất mạnh, có khả năng phản ứng với nhiều chất khác nhau, từ kim loại, oxit kim loại, đến các hợp chất hữu cơ và vô cơ. Chính vì tính chất này, HNO3 được sử dụng rộng rãi trong công nghiệp và nghiên cứu hóa học.
6.2. HNO3 làm quỳ tím chuyển màu gì?
HNO3 làm quỳ tím chuyển sang màu đỏ, thể hiện tính axit mạnh của nó. Đây là một trong những cách nhận biết đơn giản và phổ biến để kiểm tra tính axit của một dung dịch. Phản ứng này xảy ra do ion H+ trong HNO3 tương tác với chất chỉ thị màu trong giấy quỳ tím, làm thay đổi màu sắc.

Axit Nitric làm quỳ tím chuyển màu đỏ
6.3. Axit nitric có độc không?

Axit Nitric có độc không
Có, axit nitric (HNO3) là một chất độc hại, ăn mòn mạnh và dễ gây cháy. HNO3 tinh khiết thường không màu, nhưng nếu để lâu trong không khí, nó sẽ chuyển sang màu vàng nhạt do sự tích tụ của các oxit nitơ (NOx). Những nguy hiểm liên quan đến HNO3 bao gồm:
- Tính ăn mòn: HNO3 có khả năng phá hủy da, niêm mạc và các mô sống nếu tiếp xúc trực tiếp.
- Tính độc: Hít phải hơi HNO3 có thể gây kích ứng đường hô hấp, dẫn đến ho, khó thở, hoặc thậm chí tổn thương phổi nghiêm trọng.
- Khả năng gây cháy: HNO3 có tính oxy hóa mạnh, dễ dàng phản ứng với các chất dễ cháy, gây nguy cơ cháy nổ.
Axit nitric (HNO3) là một hóa chất quan trọng với nhiều ứng dụng đa dạng trong công nghiệp, nông nghiệp, và nghiên cứu. Từ việc sản xuất phân bón, thuốc nổ, đến xử lý bề mặt kim loại và tổng hợp hóa chất, HNO3 đóng vai trò thiết yếu trong việc thúc đẩy sự phát triển của nhiều ngành kinh tế. Tuy nhiên, vì tính chất độc hại và ăn mòn cao, việc sử dụng và bảo quản HNO3 cần được thực hiện cẩn thận, tuân thủ các quy định an toàn nghiêm ngặt.
Tại GH Group, chúng tôi tự hào là đơn vị cung cấp các sản phẩm hóa chất chất lượng cao, bao gồm axit nitric (HNO3), đáp ứng tiêu chuẩn an toàn và hiệu quả cho mọi nhu cầu của khách hàng. Với đội ngũ chuyên gia giàu kinh nghiệm, chúng tôi cam kết mang đến giải pháp tối ưu, từ tư vấn kỹ thuật đến cung cấp sản phẩm phù hợp với từng lĩnh vực ứng dụng.
Nếu bạn đang tìm kiếm nguồn cung cấp HNO3 uy tín hoặc cần hỗ trợ về các giải pháp hóa chất, đừng ngần ngại liên hệ với Hóa chất Gia Hoàng. Chúng tôi luôn sẵn sàng đồng hành cùng bạn trong mọi dự án và nhu cầu hóa chất của mình.
CÔNG TY TNHH THƯƠNG MẠI DỊCH VỤ XUẤT NHẬP KHẨU GIA HOÀNG
- Địa chỉ: 33/111 Tô Ký, Phường Tân Chánh Hiệp, Quận 12, TP. Hồ Chí Minh
- VPGD: 33/B4 Tô Ký, Phường Tân Chánh Hiệp, Quận 12, TP. Hồ Chí Minh
- Email: hoangkimthangmt@gmail.com
- Website: https://ghgroup.com.vn
- Hotline: 0916047878

