
Oxit axit là gì? Tính Chất, Cách Nhận Biết và Ví Dụ
17 Tháng 12, 2024
Trong lĩnh vực hóa học, oxit axit là một khái niệm quen thuộc, đóng vai trò quan trọng trong việc giải thích các phản ứng hóa học cũng như ứng dụng thực tiễn trong đời sống và công nghiệp. Là một chuyên gia hóa chất tại GH Group, chúng tôi sẽ giúp bạn hiểu rõ hơn về oxit axit là gì, từ định nghĩa, các ví dụ phổ biến, đến tính chất hóa học và cách nhận biết chúng. Đồng thời, bài viết cũng sẽ đề cập đến cách gọi tên oxit axit, giúp bạn dễ dàng áp dụng kiến thức này vào và thực tiễn.
1. Định nghĩa Oxit Axit là gì?
Đinh nghĩa về oxit axit
Oxit axit là một loại oxit được hình thành từ phi kim hoặc một số kim loại có hóa trị cao, có khả năng tham gia vào các phản ứng hóa học đặc trưng. Cụ thể, oxit axit có thể:
- Tác dụng với nước để tạo thành axit.
- Tác dụng với bazơ để tạo thành muối và nước.
Đây là một trong những nhóm oxit quan trọng trong hóa học, thường gặp trong các phản ứng vô cơ.
Ví dụ về oxit axit:
- CO2 (carbon dioxide): Tác dụng với nước tạo thành axit carbonic (H2CO3).
- SO2 (sulfur dioxide): Tác dụng với nước tạo thành axit sunfurơ (H2SO3).
- SO3 (sulfur trioxide): Tác dụng với nước tạo thành axit sunfuric (H2SO4).
- P2O5 (diphosphorus pentoxide): Tác dụng với nước tạo thành axit photphoric (H3PO4).
- N2O5 (dinitrogen pentoxide): Tác dụng với nước tạo thành axit nitric (HNO3).
Đặc điểm chung:
- Thành phần cấu tạo: Oxit axit thường được tạo thành từ phi kim liên kết với oxy. Một số oxit của kim loại có hóa trị cao (như CrO3, Mn2O7) cũng được xem là oxit axit.
- Tính chất hóa học: Khả năng tạo axit khi tan trong nước và phản ứng với bazơ để tạo muối là những đặc trưng quan trọng của oxit axit.
2. Các oxit axit thường gặp
Carbon dioxide (CO2)
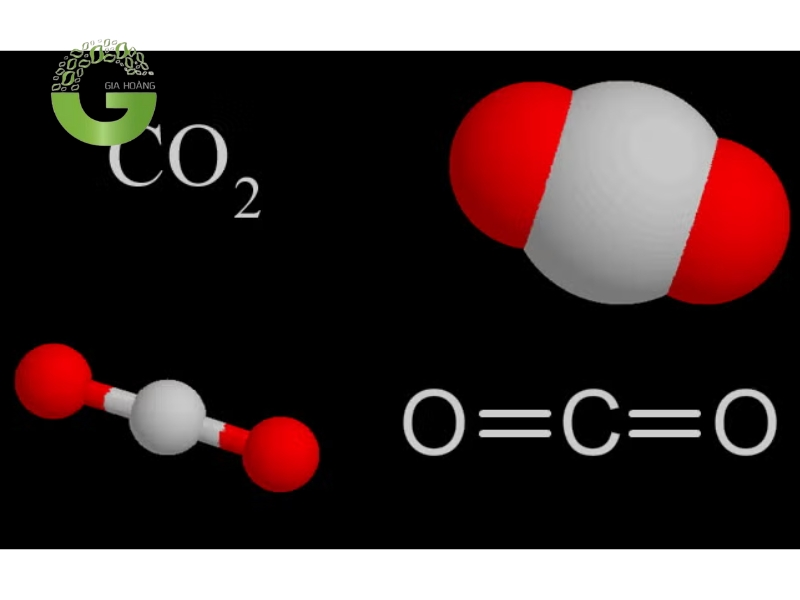
Carbon dioxide (CO2)
- Tính chất: Là một oxit axit điển hình, CO2 tan trong nước tạo thành axit carbonic (H2CO3): CO2+H2O→H2CO3
- CO2 phản ứng với bazơ để tạo muối: CO2+2NaOH→Na2CO3+H2O
- Ứng dụng: Sử dụng trong công nghiệp sản xuất nước giải khát có gas. Là nguyên liệu trong sản xuất phân bón và hóa chất.
Sulfur dioxide (SO2)
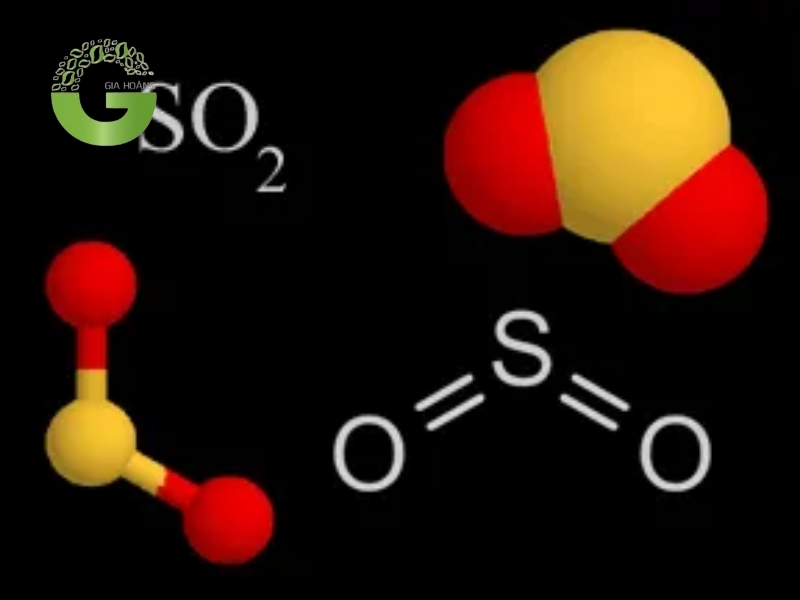
Sulfrur dioxide (SO2)
- Tính chất: Tan trong nước tạo thành axit sunfurơ (H2SO3): SO2+H2O→H2SO3
- Phản ứng với bazơ để tạo muối sunfit: SO2+2NaOH→Na2SO3+H2O
- Ứng dụng: Được sử dụng làm chất tẩy trắng trong ngành công nghiệp giấy và dệt may. Là chất khử trùng trong bảo quản thực phẩm.
Sulfur trioxide (SO3)
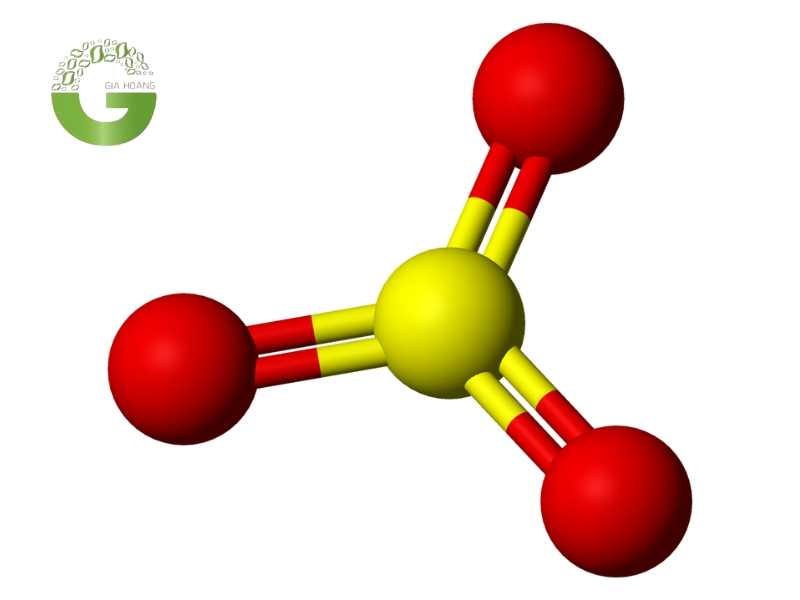
Sulfur trioxide (SO3)
- Tính chất: Tan trong nước tạo thành axit sunfuric (H2SO4): SO3+H2O→H2SO4
- Phản ứng mạnh với bazơ để tạo muối sunfat: SO3+2NaOH→Na2SO4+H2O
- Ứng dụng: Là nguyên liệu chính trong sản xuất H2SO4 98% (axit susunfur), một hóa chất công nghiệp quan trọng.
Diphosphorus pentoxide (P2O5)
Diphosphorus pentoxide (P2O5)
- Tính chất: Tan trong nước tạo thành axit photphoric (H3PO4): P2O5+3H2O→2H3PO4
- Phản ứng với bazơ để tạo muối photphat.
- Ứng dụng: Sử dụng trong sản xuất phân bón và chất tẩy rửa. Là chất hút ẩm mạnh trong phòng thí nghiệm.
Dinitrogen pentoxide (N2O5)
Dinitrogen pentoxide (N2O5)
- Tính chất: Tan trong nước tạo thành axit nitric (HNO3): N2O5+H2O→2HNO3
- Phản ứng với bazơ để tạo muối nitrat.
- Ứng dụng: Là nguyên liệu trong sản xuất axit nitric và các hợp chất nitrat.
Xem thêm: Axit nitric HNO3 là gì? Tìm hiểu tính chất và ứng dụng
3. Tính chất hóa học của Oxit Axit

Tính chất hóa học của Oxit Axit
Tác dụng với nước
Một số oxit axit tác dụng với nước để tạo thành dung dịch axit tương ứng. Đây là một trong những phản ứng đặc trưng nhất của oxit axit.
Ví dụ:
CO2+H2O⇌H2CO3
(Carbon dioxide tác dụng với nước tạo thành axit carbonic.)
SO3+H2O→H2SO4
(Sulfur trioxide tác dụng với nước tạo thành axit sunfuric.)
Lưu ý: Không phải tất cả các oxit axit đều tan trong nước. Ví dụ, SiO2 (silicon dioxide) không tan trong nước, do đó không tạo thành axit tương ứng.
Tác dụng với bazơ
Oxit axit phản ứng với dung dịch bazơ để tạo thành muối và nước. Đây là một phản ứng trung hòa điển hình, thể hiện tính chất axit của oxit axit.
Ví dụ:
CO2+2NaOH→Na2CO3+H2O
(Carbon dioxide phản ứng với natri hydroxit tạo thành hóa chất Soda (natri cacbonat) và nước.)
SO2+Ca(OH)2→CaSO3+H2O
(Sulfur dioxide phản ứng với canxi hydroxit tạo thành canxi sunfit và nước.)
Phản ứng này thường được ứng dụng trong công nghiệp, ví dụ như xử lý khí thải chứa SO2 bằng dung dịch Ca(OH)2 để giảm thiểu ô nhiễm môi trường.
Tác dụng với oxit bazơ
Oxit axit cũng có khả năng phản ứng với oxit bazơ để tạo thành muối. Đây là một phản ứng đặc trưng khác của oxit axit, thường xảy ra khi cả hai chất ở trạng thái rắn hoặc khí.
Ví dụ:
CO2+CaO→CaCO3
(Carbon dioxide phản ứng với canxi oxit tạo thành canxi cacbonat.)
SO3+Na2O→Na2SO4
(Sulfur trioxide phản ứng với natri oxit tạo thành natri sunfat.)
4. Cách nhận biết Oxit Axit

Cách nhận biết oxit axit
Thành phần cấu tạo
Oxit axit thường là oxit của phi kim, ví dụ như CO2, SO2, SO3, P2O5, N2O5.
Một số oxit của kim loại có hóa trị cao (như CrO3, Mn2O7) cũng được coi là oxit axit.
Ví dụ:
- CO2 là oxit của phi kim carbon.
- SO3 là oxit của phi kim lưu huỳnh.
Tác dụng với nước
Oxit axit có khả năng tác dụng với nước để tạo thành dung dịch axit tương ứng (đối với những oxit axit tan trong nước).
Ví dụ:
- CO2 tan trong nước tạo thành axit carbonic (H2CO3): CO2+H2O⇌H2CO3
- SO3 tan trong nước tạo thành axit sunfuric (H2SO4): SO3+H2O→H2SO4
Lưu ý: Một số oxit axit như SiO2 không tan trong nước, do đó không tạo thành axit.
Tác dụng với dung dịch bazơ
Oxit axit tác dụng với bazơ để tạo thành muối và nước. Đây là một phản ứng trung hòa điển hình, giúp nhận biết tính chất axit của oxit axit.
Ví dụ:
CO2 phản ứng với dung dịch NaOH tạo thành natri cacbonat (Na2CO3) và nước: CO2+2NaOH→Na2CO3+H2O
SO2 phản ứng với dung dịch Ca(OH)2 tạo thành canxi sunfit (CaSO3) và nước: SO2+Ca(OH)2→CaSO3+H2O
5. Tên gọi của Oxit Axit

Cách gọi tên các oxit axit
Quy tắc gọi tên oxit axit
Tên của oxit axit được hình thành theo cấu trúc:
- Tên phi kim (kèm theo tiền tố chỉ số nguyên tử nếu phi kim có nhiều hóa trị) + Oxit.
- Tiền tố chỉ số nguyên tử: Sử dụng các tiền tố như mono-, đi-, tri-, tetra-, penta-,... để chỉ số lượng nguyên tử phi kim hoặc oxy trong phân tử.
- Nếu phi kim có nhiều hóa trị, cần sử dụng tiền tố để chỉ rõ số lượng nguyên tử phi kim trong hợp chất.
Ví dụ về cách gọi tên oxit axit
- CO2: Cacbon đioxit (oxit của phi kim carbon, có 2 nguyên tử oxy).
- SO2: Lưu huỳnh đioxit (oxit của phi kim lưu huỳnh, có 2 nguyên tử oxy).
- SO3: Lưu huỳnh trioxit (oxit của phi kim lưu huỳnh, có 3 nguyên tử oxy).
- P2O5: Điphotpho pentaoxit (oxit của phi kim photpho, có 2 nguyên tử photpho và 5 nguyên tử oxy).
Một số oxit axit có tên gọi riêng
Bên cạnh tên gọi theo quy tắc, một số oxit axit còn có tên gọi riêng, thường được sử dụng trong các tài liệu khoa học hoặc công nghiệp.
- N2O3: Nitơ trioxit, còn được gọi là anhydride nitrơ.
- N2O5: Đinitơ pentaoxit, còn được gọi là anhydride nitric.
Tóm lại, bài viết trên đã trả lời cho câu hỏi oxit axit là gì và những tính chất hóa học đặc trưng của nó đóng vai trò rất quan trọng trong nhiều ngành công nghiệp và nghiên cứu khoa học. Việc hiểu rõ về nhóm hợp chất này không chỉ giúp bạn ứng dụng hiệu quả trong thực tế mà còn mở ra cơ hội trong các lĩnh vực như hóa học môi trường, công nghiệp hóa chất và giáo dục.
Nếu bạn đang tìm kiếm các sản phẩm hóa chất chất lượng cao, bao gồm các loại oxit axit và các hợp chất liên quan, GH Group chính là đối tác đáng tin cậy. Với đội ngũ chuyên gia giàu kinh nghiệm và cam kết mang lại giải pháp tối ưu, chúng tôi luôn sẵn sàng hỗ trợ bạn trong mọi nhu cầu nghiên cứu và sản xuất.
Hãy liên hệ với Hóa chất Gia Hoàng ngay hôm nay để được tư vấn chuyên sâu và nhận các sản phẩm hóa chất đạt tiêu chuẩn chất lượng cao!
CÔNG TY TNHH THƯƠNG MẠI DỊCH VỤ XUẤT NHẬP KHẨU GIA HOÀNG
- Địa chỉ: 33/111 Tô Ký, Phường Tân Chánh Hiệp, Quận 12, TP. Hồ Chí Minh
- VPGD: 33/B4 Tô Ký, Phường Tân Chánh Hiệp, Quận 12, TP. Hồ Chí Minh
- Email: hoangkimthangmt@gmail.com
- Website: https://ghgroup.com.vn
- Hotline: 0916047878

