Amoniac NH3 là một trong những hợp chất hoá học được dùng nhiều nhất hiện nay. NH3 được ứng dụng nhiều trong công nghiệp tuy nhiên chất này khá độc hại. Vậy hãy cùng chúng tôi tìm hiểu Amoniac là gì và amoniac dùng để làm gì nhé!
1. Amoniac (NH3) là gì?
Trước khi tìm hiểu amoniac dùng để làm gì? thì trước tiên chúng ta sẽ cùng tìm hiểu dung dịch amoniac là gì nhé
Amoniac là tên gọi xuất phát từ thuật ngữ amoniac trong tiếng Pháp. Amoniac là một hợp chất vô cơ được cấu tạo từ 3 nguyên tử nitơ và 1 nguyên tử hydro tạo nên 1 liên kết kém bền. Công thức hoá học của amoniac là NH3.
NH3 có cấu trúc phân tử là hình chóp, nguyên tử nitơ ở đỉnh liên kết với 3 nguyên tố hidro ở đáy.
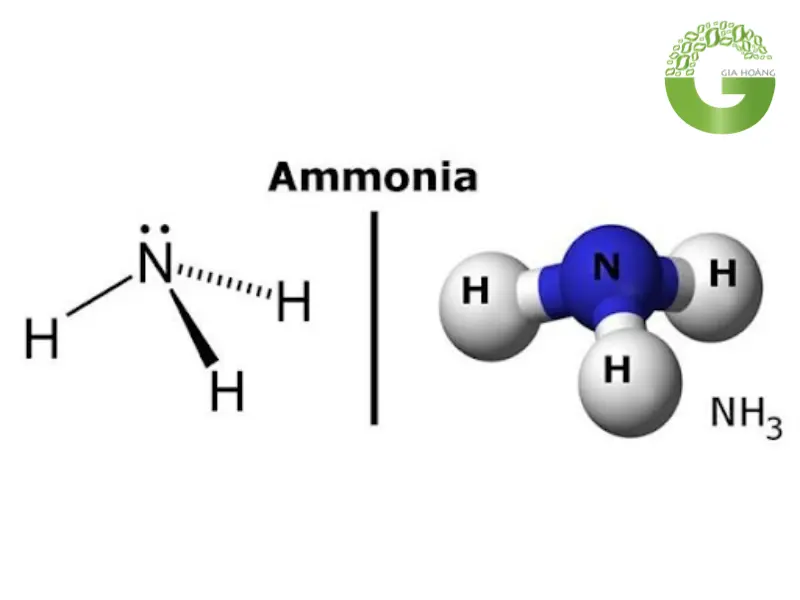
Amoniac (NH3) là gì
Amoniac được sinh ra chủ yếu ở trong tự nhiên, thận của mỗi cá nhân chúng ta cũng tạo ra một lượng nhỏ khí NH3. Vì thế nên nước tiểu cũng có mùi hôi khó chịu tương tự với khí amoniac. Khí amoniac cũng được hình thành trong quá trình phân huỷ xác động vật dưới tác dụng của vi khuẩn.
2. Tính chất hóa lý của Amoniac là gì?
2.1 Tính chất hóa học của Amoniac

Tính chất hóa học của Amoniac
- Dung dịch NH3 là một hợp chất có tính bazơ kém bền, nên nó có các tính chất hoá học của một bazơ yếu.
- NH3 tan trong nước sẽ phân huỷ thành cation amoni NH 4 +, giải phóng anion OH - theo phương trình: NH3 + H2O -> NH4 + + OH
- NH3 có tính bazơ yếu, nên sẽ làm quỳ tím ngả màu xanh
- Amoniac dễ bị oxy hoá ở nhiệt độ cao nên kém bền: 2NH3 -> N2 + 3H2N2 + 3H3 -> 2NH3
- NH3 tác dụng được với kim loại chuyển tiếp tạo ra muối phức theo phương trình: 2NH3 + Ag + -> (Ag (NH3) 2)
- Amoniac cũng có tính chất khử, nguyên tử hidro trong amoniac dễ bị thay thế bằng nguyên tử kim loại kiềm: 2NH3 + 2Na -> 2NaNH2 + H2
- Amoniac tạo ra muối amoni khi tác dụng với axit: NH3 + H + -> NH4
- NH3 có khả năng tạo kết tủa nhiều hidroxit kim loại khi tác dụng với dung dịch muối.
2.2 Tính chất vật lý của Amoniac
- Amoniac chủ yếu tồn tại dưới dạng khí, không màu và có mùi hôi thối khá khó chịu. Amoniac có thể gây tử vong nếu có nồng độ lớn. Amoniac có mật độ gấp 0,589 lần không khí và nhẹ hơn không khí.
- Vì phân tử NH3 có cặp electron tự do, và liên kết N-H bị phân cực cho nên amoniac có độ nhớt cao, theo lý thuyết thì amoniac cũng là chất dễ bị hóa lỏng.
- Amoniac là dung môi hoà tan mạnh, có hằng số hòa tan nhỏ hơn nước nên hoà tan vào dung môi hữu cơ dễ dàng hơn nước. NH3 lỏng có thể hoà tan muối và các kim loại Sr, Ca, Br tạo ra màu xanh thẫm.
- Khối lượng của một phân tử NH3 tại áp suất tiêu chuẩn 1atm là 0.769 kg/m3, với hệ số giãn nở thể tích 850 đến 1000 lần. Ở nhiệt độ -33 độ C, NH3 có khối lượng phân tử là 681 kg/m3.
- Amoniac hoà tan 47% ở nhiệt độ 0 độ C (89,0 g/100 ml), hoà tan 31% ở 25 độ C, hoà tan 18% ở nhiệt độ 50 độ C.
- Dung dịch amoniac có độ pH lớn hơn 12 nên có tính bazơ.
- Dung dịch amoniac sôi ở nhiệt độ 33,34 độ C và có điểm nóng chảy là -77,7 độ C, NH3 khí có nhiệt độ tự cháy là 650 độ C.
Xem thêm: Muối Lạnh Ammonium Chloride NH4Cl - Amoni Trung Quốc 25kg/bao
3. Quy trình sản xuất NH3 như thế nào
Amoniac là gì? Có thể điều chế được cả trong phòng thí nghiệm và trong công nghiệp hay không?
- Để điều chế amoniac trong phòng thí nghiệm như sau

Điều chế amoniac trong phòng thí nghiệm
Dùng muối NH4Cl phản ứng với dung dịch amoniac chứa Ca (OH) 2, tạo ra khí NH3
2NH4Cl + Ca (OH) 2 -> NH3 (khí) + CaCl2 + H2 (khí)
- Cách điều chế ra amoniac trong công nghiệp
Chủ yếu theo phương thức Haber - Bosch với phản ứng hai chiều liên tiếp xảy ra
CH4 + H2O <-> CO + 3H2 (nhiệt độ cao, xúc tác Ni)
N2 + 3H2 <-> 2NH3 (* tam giác * H = -92 kJ/mol)
Ngoài ra người ra cũng có thể dùng các công nghệ tiên tiến khác như: công nghệ M.W.Kellogg, công nghệ Haldor Topsoe, công nghệ Krupp Uhde, công nghệ ICI/ công nghệ Brown & Root để sản xuất amoniac.
Amoniac trong công nghiệp được bán dưới dạng khí hóa lỏng NH3 và dung dịch amoniac NH4OH, thường được lưu trữ trong ống trụ hoặc xe bồn.
Do ở dạng đậm đặc amoniac cực kỳ nguy hiểm và có tính chất ăn mòn cho nên yêu cầu về sản xuất, lưu trữ amoniac cần phải tuân thủ theo các tiêu chuẩn khắt khe.
4. Ứng dụng của muối Amoniac NH3 là gì?
Sau đây là một vài ví dụ tiêu biểu về ứng dụng NH3:
- Làm phân bón: Tất cả các hợp chất hữu cơ đều có nguồn gốc từ NH3, rất tốt đối với sự tăng trưởng của cây cối.
- Làm chất tẩy rửa trên các bề mặt như: lò nướng, thuỷ tinh, đồ gỗ và gốm, NH3 lỏng sẽ phát ra ánh sáng lấp lánh.
- Chất kháng khuẩn trong thực phẩm giúp loại bỏ nhiễm khuẩn trong thịt gia súc, amoniac cũng có tác dụng điều chỉnh độ chua.
- Amoniac cũng có thể giúp cho màu sắc của đồ gỗ sáng hơn.
- Khai thác kim loại màu như niken và molypden từ các mỏ khoáng sản, ngoài ra cũng dùng để trung hoà axit, thành phần của dầu mỏ và bảo vệ các thiết bị khỏi sự ăn mòn.
- Dùng trong xử lý khí thải với mục đích trung hòa các hợp chất như sox, nox trong khí thải của nhiên liệu hóa thạch như dầu mỏ, than, . ..

Ứng dụng của muối Amoniac (NH3) là gì
5. Lưu ý khi sử dụng Amoniac
Ở nồng độ đậm đặc cao amoniac là một khí độc. Cần chú ý nếu hít phải, ngửi phải hoặc tiếp xúc với amoniac có nồng độ quá cao có thể gây ra tình trạng ngộ độc amoniac, có thể ảnh hưởng đến sức khoẻ hoặc thậm chí là tử vong. Ở dạng dung dịch NH4OH thì amoniac là một dung dịch bazơ yếu, được chuyển hoá từ NH3 và nước.

Lưu ý khi sử dụng Amoniac
Khi dùng amoniac bạn cần chú ý như sau:
- Luôn mang quần áo bảo hộ lao động khi tiếp xúc với amoniac. Đây là chất ăn mòn có thể gây độc hại đối với da, mắt và hệ hô hấp nếu tiếp xúc trực tiếp.
- Đảm bảo rằng bạn tiếp xúc với amoniac ở khu vực có thông khí tốt nhằm giảm nguy cơ hít phải khí amoniac độc hại.
- Amoniac có thể tạo ra các hợp chất độc hại khi phản ứng với nhiều axit khác nhau, đặc biệt là axit mạnh.
- Đảm bảo lưu trữ amoniac ở nơi khô ráo, thoáng mát, và tránh tầm tay trẻ em. Bồn lưu trữ amoniac cần được đậy kín và được dán nhãn cẩn thận.
- Nếu phát hiện thấy rò rỉ amoniac ngay lập tức thông báo cho cơ quan cứu hoả hoặc cơ quan chuyên môn.
- Nếu tiếp xúc với amoniac gây ra các triệu chứng khác bao gồm đỏ da, ngứa cổ họng, hoặc khó thở. Ngay lập tức rời khỏi khu vực ô nhiễm và đến bệnh viện hoặc gọi ngay cho trung tâm kiểm soát ô nhiễm để được hướng dẫn và chữa trị.
- Đọc kĩ khuyến cáo sử dụng và hướng dẫn từ nhà sản xuất trước khi dùng amoniac.
Như vậy, chúng ta đã cùng nhau tìm hiểu chi tiết về Amoniac là gì. Nếu bạn có nhu cầu mua Amoniac thì hãy liên hệ với Hóa Chất Gia Hoàng ngay nhé. Chúng tôi sẽ hỗ trợ và tư vấn tận tình giúp bạn tìm được loại hóa chất phù hợp nhất.

















